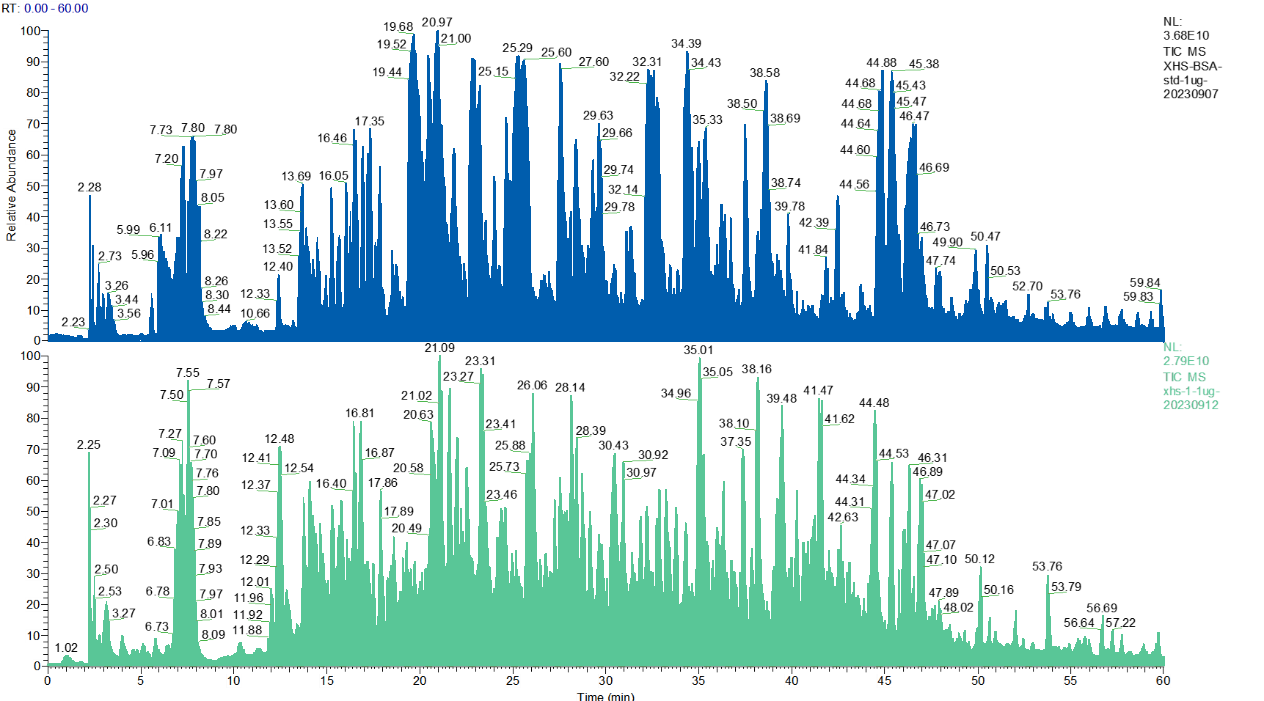
Las proteínas recombinantes se expresan principalmente en células huésped, como bacterias, levaduras, mamíferos, insectos o líneas celulares vegetales. Durante el proceso de bioproducción, estas células Huésped también producen proteínas subproductos necesarias para las funciones celulares normales. A medida que las células experimentan apoptosis, muerte y lisis, estas proteínas subproducto se liberan en el medio de cultivo celular. En consecuencia,Proteína residual de la célula huéspedConvertirse en impurezas críticas relacionadas con el proceso que pueden afectar la Seguridad clínica y la eficacia. La Farmacopea de EE. UU. Estipula que los niveles de residuos de HCP deben oscilar entre 1 y 100 ng/mg.
Los ensayos ELISA son el método farmacopeal para la cuantificación del HCP, a pesar de algunas limitaciones. Por ejemplo, la cobertura de anticuerpos en los kits ELISA es solo de aproximadamente 50% 80%, lo que significa que no puede cubrir todos los tipos de HCP. Además, ELISA solo puede medir la cantidad total de HCP y no puede proporcionar información sobre los tipos y cantidades de HCP individuales. Por lo tanto, los expertos de la industria recomiendan utilizar la espectrometría de masas para una identificación precisa y un análisis cuantitativo de los HCP como método ortogonal.
1. Optimización del bioproceso
Se realizan estudios comparativos de muestras en proceso de diferentes rutas para analizar la eficiencia escalonada de la eliminación de HCP, identificando así la ruta óptima. Dado que ELISA solo puede detectar el contenido total de HCP, algunos HCP con alto contenido pero baja inmunogenicidad (no reconocidos por anticuerpos) no se pueden controlar eficazmente. Por lo tanto, se recomienda utilizar datos de espectrometría de masas durante el desarrollo del proceso para un monitoreo más preciso.
2. Análisis de HCP en productos finales
El análisis comparativo de sustancias farmacológicas de diferentes lotes se lleva a cabo para evaluar la estabilidad del bioprocesamiento. Este análisis, combinado con los datos de ELISA, evalúa aún más las impurezas residuales de HCP y reduce los riesgos clínicos.