Los biológicos se expresan a partir de huéspedes de células bacterianas, de levadura, de animales y de líneas celulares continuas. Como los productos biológicos se producen a partir de un sustrato celular, es inevitable que el ADN residual de la célula huésped esté presente en los productos finales. Tiene riesgos potenciales de inmunogenicidad, oncogenicidad e infectividad debido al tumor o genes relacionados con virus en las líneas celulares de paso. El ADN residual tiene un riesgo potencial alto para la Seguridad y se considera un atributo de calidad crítico. Las agencias actuales, incluidas la OMS, La UE y La FDA, limitaron las cantidades aceptadas de ADN residual (menos de 10 ng o 100 pg/dosis). Entre los métodos de detección de ADN residual, la qPCR se considera el más práctico para la cuantificación de ADN residual debido a su sensibilidad, precisión, precisión y ahorro de tiempo.
Dado que el ADNr podría provenir de una amplia variedad de huéspedes, el ADNr puede existir en diferentes tamaños y formas físicas. diferentes límites de contenido y tamaño de ADN pueden ser aceptables para las agencias reguladoras si están respaldados por evidencias científicas y una evaluación de riesgos sólida. El nivel de residuos de ADN de la célula huésped puede servir como un indicador de la consistencia del producto y el control de calidad. La Detección de ADN residual garantiza la consistencia entre los lotes de producción y proporciona una referencia para la evaluación de la calidad del producto.
Para analizar la concentración de ADN de la célula huésped y la distribución de tamaño, las fracciones de ADN se extraen primero de la muestra para asegurar la detección sin compuestos inhibidores de la matriz de la muestra. La separación de perlas magnéticas es la tecnología más utilizada para este propósito, lo que permite procesos de extracción automatizados que aumentan el rendimiento y la precisión.
Para determinar la eficiencia de extracción del ADN de la célula huésped residual, se añade una cantidad conocida de ADN diana (El 'Spike') a la muestra antes de la extracción. Comparando la cantidad de ADN medida después de la extracción con la cantidad de picos, se puede calcular la eficiencia de extracción. Este Valor de eficiencia se usa a continuación para determinar el ADN de la célula huésped residual en la muestra. Una reducción en la eficiencia de extracción indica la presencia de compuestos inhibidores coextraídos con el ácido nucleico.
El desarrollo de un método de detección altamente sensible y específico para el ADN de la célula huésped utilizando PCR en tiempo real requiere un diseño de cebador cuidadoso y una optimización de la reacción de PCR. La especificidad y la sensibilidad dePCR en tiempo realEstán influenciados por la temperatura de recocido, el tiempo y las concentraciones de cationes y cebadores en el tampón de reacción. Dirigirse a un gen presente en múltiples copias puede aumentar la sensibilidad del ensayo.
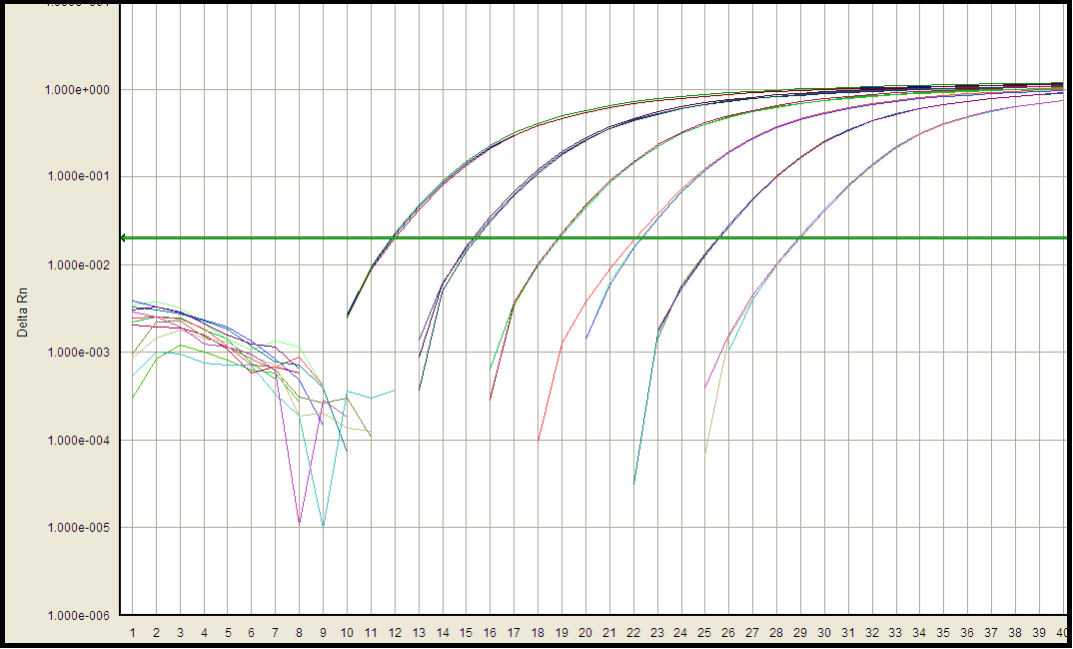
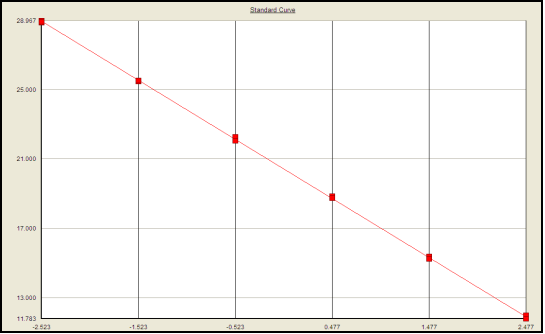
La linealidad y el rango de los métodos de ensayo se evaluaron calculando la línea de regresión de la curva estándar. La precisión se evaluó analizando el porcentaje de recuperación de los estándares de ADN con picos en tres concentraciones diferentes. La precisión del intraensayo y entre ensayos se evaluó mediante el % de CV DE TODAS LAS QC en cada nivel. La sensibilidad se determinó comprobando el LOD y el LLOQ. La especificidad se evaluó analizando muestras de ADN o un conjunto de ADN de matriz extraído de la especie/cepa relevante. La robustez se evaluó evaluando la estabilidad del rendimiento del ensayo bajo diferentes condiciones de almacenamiento.
El Alcance de validación del ensayo de ADN de la célula huésped residual incluye:
Exactitud
Precisión
Especificidad
Límite de cuantificación (LOQ)
Linealidad
Rango
Robustez
Un ensayo totalmente validado permite el uso de productos disponibles comercialmente o kits diseñados específicamente dirigidos a la secuencia de ADN del huésped, haciéndolo aplicable para pruebas entre productos biológicos.
Estudio de caso-Cuantificación residual del ADN de células huésped
CHO HCD rendimiento de validación-
Curva estándar: 96.6% de eficiencia de amplificación, 0.999 de coeficiente de correlación